Вте
За даними метааналізу ризику смерті від усіх причин та масивних кровотеч в осіб із ЛЕ, незалежно від її типу (стабільна або нестабільна), тромболітична терапія значно знижує загальну летальність порівняно з антикоагулянтною терапією. Водночас, у пацієнтів зі стабільною ЛЕ застосування тромболізісу пов’язане зі зменшенням смертності, але підвищенням показника масивних кровотеч, особливо у віці >65 років, порівняно з призначенням лише антикоагулянтів (Chatterjeeet al., 2014).
Фібриляція передсердь, когнітивна дисфункція, цереброваскулярні ушкодження та інсульт: що спільного?
Як зазначають дослідники, однією з переваг є плейотропні ефекти НОАК, зокрема, додатковий протизапальний ефект: знижуючи рівень С-реактивного протеїну й інтерлейкіну‑6, вони чинять вплив на ендотеліальну дисфункцію, що особливо важливо для пацієнтів із патологією нирок (Russo and Fabiani, 2022).
Отже, основні нагальні питання пов’язані з профілактикою у хворих, що отримують системну хіміотерапію, а також лікуванням онкологічних хворих із ВТЕ. Власне, профілактика є запорукою виживання пацієнтів, які госпіталізовані з онкопатологією (мають активне онкозахворювання або онкологічний анамнез), проходять оперативне втручання з приводу онкопатології або отримують амбулаторне лікування. Слід зазначити, що тривалість АКТ, насамперед низькомолекулярними гепаринами (НМГ), визначається не іммобілізацією пацієнта і тривалістю госпіталізації. За агресивних форм раку НМГ застосовують упродовж 30-35 днів; ВТЕ мають приймати НОАК (апіксабан і ривароксабан) (апіксабан чи ривароксабан).
ПОАК слід віддавати перевагу перед антагоністами вітаміну К на початку застосування пероральних антикоагулянтів в осіб із ЛЕ, яким показане приймання ПОАК, як-то апіксабан, дабігатран, едоксабан, ривароксабан (І, А). При цьому ПОАК не рекомендовано призначати хворим із тяжким порушенням функції нирок, під час вагітності та лактації, а також пацієнтам з антифосфоліпідним синдромом (ІІІ, С).
Варто також зауважити, що НМГ залишаються основою лікування: їх широко застосовували для лікування гострої ТЕЛА з 2003 р. (дослідження CLOT, Lee et al., 2003) до грудня 2017 р., коли вперше було опубліковано дані дослідження НОАК. Так, згідно з рекомендаціями пацієнти мали приймати НМГ до 6 міс., що було вкрай незручно і призводило до певних місцевих ускладнень. Натомість із появою НОАК ситуація змінилася на краще, оскільки в пацієнтів з’явився вибір: НОАК або НМГ. Як відомо, пацієнти більш прихильні до НОАК, але ці препарати не застосовують за наявності раку шлунка або верхніх відділів шлунково-кишкового тракту. Своєю чергою, антагоністи вітаміну К (АВК) є незадовільними щодо взаємодії з багатьма хіміотерапевтичними препаратами і варіабельністю міжнародного нормалізованого співвідношення (МНС).
Отже, у підгрупі пацієнтів із раком ШКТ едоксабан на 3,5% знижував ризик повторної ВТЕ та на 7,9% підвищував імовірність великої кровотечі. Тому в останніх рекомендаціях Європейського товариства кардіологів (ESC) щодо лікування ТЕЛА вказано не можливість призначення едоксабану (як альтернативи для НМГ) при онкоасоційованому тромбозі лише у пацієнтів, які не мають злоякісного новоутворення ШКТ [3].
У дослідженні AMPLIFY (n=5395) пацієнтів із гострою ВТЕ рандомізували для отримання 6-місячного курсу апіксабану або еноксапарину з подальшим застосуванням варфарину. Було показано, що за ефективністю апіксабан не поступався НМГ та варфарину, натомість на тлі лікування апіксабаном ризик великих кровотеч був на 69% нижчим (Agnelli et al., 2013). За даними ретроспективного аналізу, як масивні кровотечі, так і рецедиви ВТЕ та пов’язана із ВТЕ смертність були меншими у групі апіксабану, починаючи з 7-го дня терапії.
Після лікувального парентерального етапу, тривалість якого становить у середньому 5‑7 днів, більшість пацієнтів переводять на приймання пероральних антикоагулянтів. ПрОАК (апіксабан, дабігатран, едоксабан, ривароксабан) є препаратами вибору для даної фази терапії. Вони мають порівнянну з варфарином ефективність щодо попереджання повторних ВТЕ та смерті, але асоційовані з суттєво (приблизно на 40%) нижчим ризиком геморагічних ускладнень [6]. Тому антагоністи вітаміну К (АВК) для вторинної профілактики ВТЕ на даний час перейшли у категорію препаратів другої лінії.
Так, у пацієнтів із ФП основою профілактики є призначення ОАК, які за ефективністю не відрізняються від варфарину. Зокрема, апіксабан не поступається варфарину як у первинній, так і у вторинній профілактиці (ARISTOTLE, 2012).
Прихильність до лікування – ключ до терапевтичного успіху
Своєю чергою, предикторами дотримання АКТ у пацієнтів із гострою ТЕЛА є тип антикоагулянту (для апіксабану прихильність є трохи більшою, ніж для ривароксабану, тоді як для еноксапарину або в разі зміни ОАК вона зменшується), а також безпосередні візити до лікаря (на відміну від онлайн / телефонних консультацій).

Керівник відділу клінічної фармакології та кардіоонкології, керівник центру кардіоонкології ДУ «ННЦ «Інститут кардіології, клінічної та регенеративної медицини ім. акад. М.Д. Стражеска НАМН України, д.мед.н. Сергій Миколайович Кожухов
Тривалість лікування антикоагулянтами при ТЕЛА та ТГВ має становити щонайменше три місяці. ПОАК, зокрема апіксабан та ривароксабан, застосовують у вигляді монотерапії, уникаючи призначення НМГ на початковій стадії ВТЕ. Щодо безпеки терапії ПОАК, ризик великих кровотеч є нижчим порівняно з варфарином (Schulman et al., 2014).
Інструментом для оцінювання ризику розвитку тромбозу глибоких вен (ТГВ) і ТЕЛА в онкохворих є валідована шкала KHORANA (Sanfilippo, 2022). Якщо пацієнт за цією шкалою має ≥2 балів, він потребує призначення оральних антикоагулянтів (ОАК) із профілактичною метою. Відсоток виникнення ускладнень залежить від локалізації раку, наприклад, за раку підшлункової залози або шлунка ускладнення виникають у кожного п’ятого пацієнта, що свідчить про важливість такої профілактики.
2. Великі кровотечі мали місце у 6,9% хворих на тлі використання едоксабану та 4% – дальтепарину. Ця різниця була переважно зумовлена збільшенням кровотеч в осіб із раком ШКТ.
Своєю чергою у 12-місячному рандомізованому подвійному сліпому дослідженні AMPLIFY-EXT (n=2482) порівнювали дві дози апіксабану (2,5 та 5 мг двічі на добу) із плацебо у хворих на ВТЕ, які пройшли 6‑12 місяців антикоагуляційної терапії (Agnelli et al., 2013). Симптоматична рецидивна ВТЕ або смерть від ВТЕ мала місце у 73 з 829 пацієнтів групи плацебо порівняно із 14 з 840, які отримували 2,5 мг апіксабану, та 14 з 813 – 5 мг апіксабану. Частота серйозних кровотеч становила 0,5% у групі плацебо, 0,2 та 0,1% – 2,5 і 5 мг апіксабану відповідно. Клінічно значущих незначних кровотеч було 2,3% на тлі застосування плацебо, 3% – 2,5 мг апіксабану та 4,2% – 5 мг апіксабану. Рівень смертності від будь-якої причини був 1,7% у групі плацебо порівняно з 0,8 та 0,5% – 2,5 і 5 мг апіксабану відповідно.
У більшості пацієнтів із ТЕЛА на етапах діагностичного пошуку і первинної оцінки ступеня тяжкості захворювання доцільно призначати парентеральну АКТ. Препаратами вибору на цьому початковому етапі є низькомолекулярні гепарини (НМГ) або фондапаринукс у лікувальних дозах [4, 5]. У хворих на ТЕЛА високого ризику пріоритетним вважається застосування внутрішньовенного нефракціонованого гепарину (НФГ) під контролем активованого тромбопластинового часу, а НМГ розглядають як альтернативні препарати.
Своєю чергою, головними цілями Європейського плану дій щодо інсульту на 2018‑2030 рр. є зниження кількості інсультів на 10%, госпіталізація і лікування 90% пацієнтів в інсультному блоці, створення Національного плану дій, реалізація національних стратегій із залученням усіх галузей і рівнів тощо. Водночас велике значення надається не лише первинній, а й вторинний профілактиці, оскільки, як відомо, кожен четвертий мозковий інсульт є повторним.
Онкоасоційовані тромбози у практиці лікаря-кардіолога: результати дослідження CARAVAGGIO
Крім того, слід звернути увагу на те, що пацієнти віком до 65 років із ВТЕ і ТЕЛА мають вищі показники прихильності до лікування ОАК, тоді як хворі, що палять, демонструють меншу комплаєнтність (Colavecchia et al., 2022).

Нові оральні антикоагулянти (НОАК) широко використовують у пацієнтів із венозною тромбоемболією (ВТЕ), також вони є стандартом лікування і профілактики інсульту в разі неклапанної фібриляції передсердь (ФП), а також засобом терапії гострої ВТЕ з ураженням кінцівок і тромбоемболії легеневої артерії (ТЕЛА). Зокрема, за призначення антикоагулянтної терапії (АКТ) пацієнтам із ВТЕ з метою як лікування, так і профілактики, виникає багато запитань, що потребують розгляду деяких особливостей ведення окремих категорій пацієнтів.
Своєю чергою, відповідно до рекомендацій щодо лікування гострої фази за проміжного або низького ризику ЛЕ, слід ініціювати антикоагулянтну терапію без зволікань у пацієнтів із високою або проміжною клінічною ймовірністю ЛЕ, поки триває встановлення діагнозу (І, С). Якщо антикоагулянтну терапію розпочато з парентерального введення, для більшості хворих замість НФГ рекомендовано НМГ або фондапаринукс (І, А) (ESC, 2019).
Сьогодні існує доказова база щодо застосування ривароксабану й апіксабану як засобів профілактики. У дослідженні AVERT апіксабан застосовували у профілактичних дозуваннях, що сприяло зменшенню частоти виникнення епізодів ВТЕ і не супроводжувалося збільшенням ризику кровотечі протягом періоду лікування (Carrier et al., 2019). Ці дані стали підґрунтям для останніх рекомендацій із профілактики ВТЕ під час антиракової терапії. Отже, згідно з рекомендаціями NCCN та АSН (2021) амбулаторні онкологічні пацієнти з високим ризиком ВТЕ мають приймати НОАК (апіксабан і ривароксабан); також можливо розглянути НМГ (клас рекомендації ІІb, рівень доказовості B). Пацієнтам після оперативних втручань рекомендовано НМГ терміном до 4 тиж. (клас рекомендації І, рівень доказовості B) (Streiff et al., 2021).
Протягом тривалого часу препаратами вибору для цієї категорії хворих вважалися НМГ. За даними п’яти рандомізованих клінічних досліджень, тривала терапія НМГ упродовж 3‑6 місяців при онкоасоційованому тромбозі порівняно із комбінацією НМГ (5‑10 днів) + АВК супроводжувалася зниженням ризику рецидивів ВТЕ на 40% за подібної кількості великих кровотеч на тлі двох режимів лікування [17].
Останнім часом активно вивчається використання ПрОАК у цієї когорти пацієнтів – як для початкової терапії, так і після використання НМГ. У дослідженні Hokusai-VTE Cancer (n=1046) едоксабан показав порівнянну із дальтепарином (НМГ) ефективність щодо попереджання первинної комбінованої кінцевої точки, як-то рецидив ВТЕ / велика кровотеча протягом 12 місяців спостереження (ВР 0,97; 95% ДI 0,70‑1,36) [18]:
Проблема ВТЕ у практиці лікаря-кардіолога стала ще актуальнішою через пандемію COVID‑19. Міжнародні товариства рекомендують хворим, які вже отримують антикоагулянтну терапію антагоністами вітаміну К або ПОАК, продовжувати поточну антикоагуляцію або переходити на НМГ. У пацієнтів, у котрих немає проблем із прийманням пероральних ліків, або ж вони здатні перейти на ПОАК у міру поліпшення стану, можна розглянути використання ПОАК, якщо не передбачено інвазивних процедур та призначення препаратів, що потенційно взаємодіють із ПОАК.
Якщо все ж таки прийняте рішення призначити АВК, лікування слід починати паралельно з іншим антикоагулянтом (НМГ, ПрОАК тощо), відміна якого можлива тільки після досягнення міжнародного нормалізованого відношення (МНВ) у межах 2,0‑3,0 протягом принаймні двох днів поспіль. Подальша терапія АВК вважається ефективною та безпечною, лише якщо понад 70% вимірювань МНВ знаходяться у вказаному інтервалі.
В обсерваційному дослідженні (n=600 000, 4 роки) вивчали, чи є різниця щодо ризику серйозних ішемічних або геморагічних подій у пацієнтів із ФП, які отримували ривароксабан або апіксабан. Було встановлено, що в пацієнтів із ФП старше 65 років, які отримували ривароксабан, ризик ішемічних або геморагічних подій був на 20% вищий, а ризик смерті – на 6% вищий порівняно з тими, хто приймав апіксабан. Отже, дослідники дійшли висновку, що апіксабан має бути препаратом вибору для осіб зазначеного віку з ФП, оскільки застосування ривароксабану асоціювалося з підвищеним ризиком великих ішемічних або геморагічних подій (Ray et al., 2021).
Ключові принципи лікування ВТЕ
Підготувала Олександра Демецька

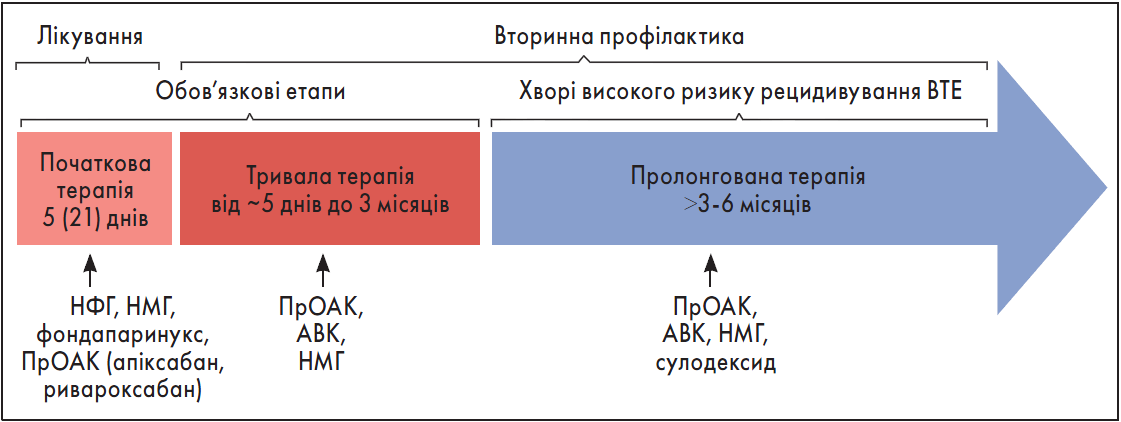
Рисунок. Фази антикоагулянтної терапії при ВТЕ
Статтю надруковано за підтримки компанії «Пфайзер»
Відповідно до настанов Європейського товариства кардіологів (ESC), антикоагулянтну терапію слід розпочинати якомога раніше. Пацієнтам із підозрою на ЛЕ групи високого ризику рекомендовано негайно розпочати внутрішньовенну антикоагулянтну терапію з нефракціонованим гепарином (НФГ), включно із болюсною ін’єкцією, скорегованою за масою тіла (І, С).
Тривалість АКТ у пацієнтів з онкологічними захворюваннями з катетер-асоційованою ВТЕ становить щонайменше 3 міс. та має бути подовжена, якщо катетер залишається на місці (ESC, 2022).
Забезпечити ефективність та безпеку втручань першочергово допомагає своєчасна та належна діагностика, зокрема за дворівнею шкалою Веллса (Spampinato et al., 2020). Якщо є підозра на ТЕЛА, необхідно провести комп’ютерно-томографічну ангіографію / пульмографію та визначитися із методами лікування.
Аналіз ефективності й безпеки терапії едоксабаном у пацієнтів із ВТЕ
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 3 (76) 2021 р.

Отже, препаратами вибору для вторинної профілактики ВТЕ (крім вагітних та деяких пацієнтів зі злоякісними новоутвореннями, особливо шлунково-кишкового тракту [ШКТ]) є ПрОАК. У межах клінічних дослідженнь були протестовані такі препарати, як:
Стаття у форматі PDF
Таким чином, було зроблено висновок, що антикоагуляція апіксабаном як у терапевтичній (5 мг), так і тромбопрофілактичній дозі (2,5 мг) знижує ризик повторних ВТЕ без підвищення частоти серйозних кровотеч.
Що стосується прихильності до лікування, то в разі призначення НОАК для первинної профілактики ВТЕ рекомендовано обговорити з пацієнтом відносну користь і шкоду, прогноз раку, вартість ліків і тривалість терапії (клас рекомендації І, рівень доказовості С). Метою є досягнення найкращого використання пацієнтами відповідних ліків, щоб максимізувати вигоду та звести до мінімуму ризик заподіяння шкоди. До цього процесу слід обов’язково залучати родину, опікунів і медичних працівників первинної або вторинної ланки. Зниження використання ОАК асоціюється зі збільшенням ризику інсульту. Наприклад, зафіксовано високі показники припинення застосування препарату із часом: близько 30% пацієнтів, що потребують ОАК, упродовж 2 років припиняють приймати будь-які ліки. Загальні показники антикоагуляції в осіб похилого віку з ФП коливаються в межах 25‑75%. Тож прихильність є дуже важливим чинником якості лікування та його ефективності. Найнадійнішим методом оцінювання прихильності до лікування є терапевтичний моніторинг, який передбачає контроль лікарем належного застосування призначених препаратів під час кожного візиту через спілкування з пацієнтом (Vrigens et al., 2005).
Натепер тривають масштабні рандомізовані дослідження застосування апіксабану в осіб із COVID‑19. Отримані результати можуть сприяти перегляду вітчизняного протоколу щодо дозволу їх використання у госпіталізованих пацієнтів.
Венозні тромбоемболії у практиці лікаря-кардіолога
Варто зауважити, що до 50% хворих на рак можуть мати ознаки безсимптомного ТГВ/ТЕЛА (Johnson et al., 1999). В онкологічних пацієнтів із симптоматичним ТГВ спостерігається високий ризик рецидиву ТГВ/ТЕЛА, що зберігається протягом багатьох років.

За словами екс-міністра охорони здоров’я США Сі Еверета Купа, ліки не діють на пацієнтів, які їх не приймають, і з цим важко не погодитися. Ефективна терапія передбачає прихильність пацієнта до медичного препарату та ефективне управління перебігом захворювання. Натомість пацієнти можуть не розпочинати призначене лікування, відкладати, пропускати прийом ліків або, навпаки, вживати додаткові дози, чи взагалі не дотримуватись рекомендацій лікаря.
Завідувачка спеціалізованого відділення аритмій серця, старша наукова співробітниця ДУ ННЦ «Інститут кардіології, клінічної та регенеративної медицини ім. акад. М.Д. Стражеска» НАМН України, к.мед.н. Таїсія Вячеславівна Гетьман
Незважаючи на відзначену останнім часом тенденцію до зниження, госпітальна летальність при цьому захворюванні досі на високому рівні – у межах від 8 до 12%. Окрім ТЕЛА, ще одним грізним ускладненням ТГВ є посттромбофлебітичний синдром, який суттєво обмежує якість життя пацієнтів, а у складних випадках може стати причиною ампутації кінцівки або смерті.
Таким чином, на фармринку України з’явився ще один ПрОАК едоксабан (Едоксакорд, 30 та 60 мг, АТ «Київський вітамінний завод»), який має потужну доказову базу щодо використання для лікування та вторинної профілактики ВТЕ, зокрема у пацієнтів з онкоасоційованим тромбозом (окрім новоутворень у ШКТ). Застосування препарату слід розпочинати після ініціальної парентеральної АКТ. Перевагами едоксабану є можливість приймання один раз на добу та проведення корекції дози (єдиний ПрОАК при терапії ВТЕ) залежно від індивідуальних характеристик хворого.
Дослідники дійшли висновку, що пероральний апіксабан не поступався підшкірному дальтепарину для лікування онкоасоційованих ВТЕ, до того ж не спостерігалося достовірного збільшення серйозних кровотеч, особливо із ШКТ. Таким чином, результати CARABAGGIO дають підстави для розширення застосування ПОАК, зокрема апіксабану, в осіб з онкоасоційованими ВТЕ, включно з раком ШКТ.
Висновки
Застосування ПОАК для лікування онкоасоційованих ВТЕ вперше вивчали у дослідженнях Hokusai VTE-Cancer (ендоксабан vs дальтепарин) та SELECT-D (ривароксабан vs дальтепарин) (Raskob et al., 2018; Young et al., 2018). Було встановлено, що у пацієнтів із/без раку шлунково-кишкового тракту (ШКТ) часто виникали шлунково-кишкові кровотечі (Kraaijpoel et al., 2018). Тож автори випробування ADAM‑VTE сфокусували увагу на аналізі безпеки апіксабану при лікуванні пацієнтів із ВТЕ. Первинною кінцевою точкою були великі кровотечі, вторинною – рецидив ВТЕ. У групі апіксабану (n=145) великі кровотечі не спостерігалися, тоді як на тлі використання дальтепарину (n=142) їх частота становила 4,4%. Щодо вторинної кінцевої точки, апіксабан сприяв зменшенню рецидивів ВТЕ (0,7%) порівняно із контрольною групою (6,3%). Крім того, якість життя хворих була кращою при застосуванні апіксабану (McBane et al., 2020).

Так, реальність під час застосування АВК полягає в тому, що 38% пацієнтів, яким призначено лікування, не починають АКТ, 36% пропускають прийом більш ніж 20% дозувань, 4% вживають понад 10% додаткових доз. Своєю чергою, погана прихильність до лікування чинить суттєвий вплив на контроль антикоагуляції. Лікування пацієнтів із ВТЕ зазвичай є тривалим. Гостре лікування продовжується не менш ніж 3 міс., інколи – понад 6 міс. Втім, за статистикою, 30% пацієнтів не продовжують лікування протягом першого року. Відповідно до рекомендацій у пацієнтів із ВТЕ, які потребують постійної АКТ, зокрема особи без онкологічного захворювання, потребують продовження терапії більш ніж на 3 міс., довготривалість якої (невизначено довго) слід розглянути у разі:
За даними проведених досліджень, якщо хворі припиняють приймати АКТ після ВТЕ, ризик повторних подій є дуже високим: протягом 10 років рецидив ВТЕ можливий у 40% чоловіків і в 30% жінок (ESC, 2021).
Основою лікування ВТЕ є антикоагулянтна терапія (АКТ), яку слід починати якомога раніше ще на етапі діагностики (тільки при підозрі на ВТЕ) і проводити щонайменше протягом трьох місяців (за відсутності протипоказань) [3]. АКТ має декілька етапів. Початковий (або лікувальний) триває залежно від обраного антикоагулянту від 5 до 21 дня. На цій стадії можуть застосовуватися парентеральні препарати або ж прямі оральні антикоагулянти (ПрОАК) ривароксабан чи апіксабан у терапевтичних дозах. Подальша АКТ спрямована на профілактику повторних ВТЕ. Вона включає обов’язковий для всіх пацієнтів етап тривалої терапії (до трьох місяців) та у деяких хворих – пролонгованого лікування (рисунок).
Подальший аналіз результатів дослідження продемонстрував, що розвиток первинної кінцевої точки у пацієнтів із раком ШКТ спостерігався у 19,4% тих, хто отримував едоксабан, і 15% – дальтепарин: різниця ризику (PP) 4,4%; 95% ДІ від -4,1 до 12,8%) [19]. Показники на тлі терапії едоксабаном та дальтепарином для раку легень становили 10,4 і 10,7% (PP -0,3%; 95% ДІ від -10 до 9,5%), для раку сечостатевої системи – 13,6 і 12,5% (PP 1,1%; 95% ДІ від -10,1 до 12,4), для раку молочної залози – 3,1 і 11,7% (PP 8,6%; 95% ДІ від -19,3 до 2,2), для гематологічних злоякісних пухлин – 8,9 і 10,9% (PP -2%; 95% ДІ від -13,1 до 9,1) та для гінекологічного раку – 10,4 і 17,4% (PP -7%; 95% ДІ від -19,8 до 5,7) відповідно.
Отримані дані сприяли перегляду рекомендацій щодо лікування онкоасоційованих тромбоемболій. Так, про доцільність терапії апіксабаном у дозі 10 мг двічі на добу протягом семи діб із наступним переходом на 5 мг два рази на день протягом принаймні шести місяців йдеться у настанові Національної комплексної онкологічної мережі США (NCCN, 2020). Також у рекомендаціях Американського гематологічного товариства (ASH, 2021) зазначено, що для початкового лікування хворих на рак та ВТЕ слід призначати ПОАК (апіксабан чи ривароксабан) або НМГ. Для застосування протягом 3‑6 місяців у онкопацієнтів із ВТЕ перевагу варто надавати ПОАК (апіксабану, едоксабану чи ривароксабану) перед НМГ.
Література
Керівник відділу клінічної фармакології та кардіоонкології ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України (м. Київ), д. мед. н. Сергій Миколайович Кожухов зазначив, що частота ВТЕ в онкологічних пацієнтів у п’ять разів перевищує таку в загальній популяції. ВТЕ є другою за значущістю причиною смерті серед госпіталізованих хворих на рак (Schmaier et al., 2018). Ризик ВТЕ в осіб із онкопатологією, що перенесли оперативне втручання, у 3‑5 разів вищий, ніж у пацієнтів без раку (Donati et al., 1994).
Тому важливою є як профілактика рецидивів, так і прихильність хворих до лікування. Для лікування ВТЕ і зниження ризику рецидиву апіксабан призначають у дозі 10 мг двічі на добу протягом 7 днів для покриття початкового періоду високого ризику, який охоплює НМГ (Buller et al., 2008).
Апіксабан, едоксабан чи ривароксабан рекомендовані для лікування симптомної або випадкової ВТЕ у пацієнтів із раком без протипоказань (клас рекомендації І, рівень доказовості А) (NCCN, 2020).
Іноді може виникати потреба у подовженні застосування антикоагулянтів протягом більш ніж трьох місяців (пролонгована фаза терапії). Таке рішення приймають на підставі оцінки тромботичних та геморагічних ризиків для кожного конкретного пацієнта. Надалі доцільність призначення АКТ слід визначати що 3‑4 місяці [3].
1. Повторна венозна тромбоемболія виникла у 7,9% пацієнтів групи едоксабану та 11,3% – дальтепарину (-3,4%; 95% ДІ від -7,0 до 0,2).
Зазначені новітні дані увійшли до вітчизняних клінічних рекомендацій із профілактики та лікування ВТЕ в осіб із онкопатологією (Кожухов та спіавт., 2020).
Венозні тромбоемболії в онкологічних хворих: від рекомендацій із кардіоонкології до клінічної практики
Отримані результати стали підґрунтям для проведення проспективного рандомізованого дослідження CARAVAGGIO (апіксабан vs дальтепарин), а саме:
Апіксабан по 5 мг двічі на добу впродовж 6 міс. – найнижча ефективна лікувальна доза з огляду на наявність тромбу. Після порівняння з плацебо двох доз апіксабану протягом 6‑12 міс. встановлено, що доза 2,5 мг двічі на добу є ефективною для профілактики, тоді як 5 мг двічі на добу – ефективна для лікування (Agnelli et al., 2013).
Щодо профілактики інсульту в пацієнтів із ФП, то апіксабан у дозуванні 5 мг двічі на добу обрано для підвищення ефективності захисту від інсульту та пов’язаної з ним смертності.
Зважаючи на передбачувану біодоступність та фармакокінетику цих ліків, ПрОАК можуть призначатися у фіксованих дозах та не потребують лабораторного контролю. Додатковими перевагами цих препаратів є швидкий початок/припинення дії та менш значуща взаємодія з іншими медикаментами і продуктами харчування, ніж у АВК.
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 6 (79) 2021 р.
Рецидив ВТЕ стався у 32 з 576 пацієнтів групи апіксабану та у 46 з 579 – дальтепарину. Великі кровотечі спостерігалася у 3,8 та 4% хворих при використанні апіксабану та дальтепарину відповідно. Великі ШКТ-кровотечі мали місце в 1,9% учасників у групі апіксабану та 1,7% – дальтепарину; великі неШКТ-кровотечі були зафіксовані у 1,9 та 2,2% пацієнтів відповідно. Летальні епізоди кровотеч були відсутні в обох групах. Загалом апіксабан зменшував рецидиви ВТЕ на 37% (Agnelli et al., 2020).
Источники:
https://empendium.com/ua/chapter/B27.II.2.33.1.&rut=3bf97004f7a48e3614e4107399319a7815a8525e92bdde5355c13ed1a7dbf58c
https://www.youtube.com/watch?v=Fm5iP0S1z9w&rut=8734463e051931da6b02ed3785224512c6869643635ecb4e3447f2562619c21a
https://health-ua.com/cardiology/tromboz/66562-suchasn-pdhodi-dolkuvannya-venozno-tromboembol&rut=38bb2e13f8b1f10d12c0e73e800d70c1022d38387ae89dee398cfc7669c9ef37
https://pluton.ua/p/brochures/doc/Thyristor_exciters_VTE,VTP_ua.pdf&rut=54bc1229c046e80c5c2f537f09f596cc418d918eff6e45cca4726eb4e8723c0a
https://health-ua.com/cardiology/tromboz/69021-antikoagulyantna-terapya-venoznih-tromboembolj-ufokus-edoksaban&rut=56756c85d0af2f0966c50fe66b1c730deeffb3ce41058050d065801ae212b3ad
https://health-ua.com/cardiology/kardiovaskuliarna-profilaktika/72214-antikoagulyantna-terapya-nagaln-pitannya—lkuvannya-proflaktiki-taprihilnos&rut=b21cbc1aea9bd6df1b5e9ad3a979ce99b3d946faf885287dffd218de9805c1a6
https://empendium.com/ua/chapter/B27.II.2.33.2.&rut=10f928ac1be7a55e7431d5fa5f0363f20df1210bdf7f8f35a5ec82ad7ec3b411
https://sel.vtei.edu.ua/&rut=8e81aecfda52b3328f45ce8ec8498483cbf6ed86e1d20ff6291d9c85602959a3
https://empendium.com/ua/chapter/B27.8.3.118.&rut=3f59d70e0f4ea7e3e9da311b87572c7016f585b062e7bdf7900f5bbaf0759914
